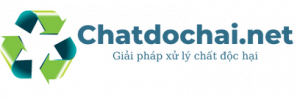Amoni Nitrat – một chất hóa học không còn lạ lẫm gì với nhiều người, nhất là những người làm trong lĩnh vực hóa học và nông nghiệp. Thực chất, đây là một hợp chất với khá nhiều cách sử dụng. Bạn có thể thấy thành phần này trong phân bón. nhưng cũng có thể thấy sự xuất hiện của nó trong một số vụ nổ kinh hoàng. Tại sao lại có sự khác biệt lớn giữa ứng dụng của nó như vậy, hãy cùng tìm hiểu các tính chất là sẽ rõ.
Giải thích về NH4NO3 – Amoni Nitrat
Hợp chất này tồn tại trên Trái đất với hai nguồn: từ tự nhiên và từ các phản ứng hóa học. Có thể nhiều người sẽ thấy bất ngờ khi hóa chất này lại có sẵn trong tự nhiên. Thực chất, có thể tìm thấy Amoni Nitrat tại Chile, cụ thể là sa mạc Atacama.
Trước đây, người ta phát hiện tại sa mạc này có một lượng lớn Nh4NO3 và khai thác từ nó. Tuy nhiên hiện nay, con người không tốn công vào việc khai thác nữa mà trực tiếp tạo ra hợp chất này.
Như đã biết, công thức hóa học của hợp chất là Amoni Nitrat, hợp chất này có tính muối trung hòa, được nhìn thấy bằng mắt thường với những hạt tinh thể màu trắng. Nó được tạo ra từ quá trình cho axit nitric tác dụng với amoniac. Hợp chất này có thể hút hơi ẩm và tan khi cho vào trong nước.
Bên cạnh đó, một vài tên gọi khác của nó là Ammonium Nitrate, Amoni Nitrate, Nitrat Amon,… Hiện nay, loại hóa chất này đang được sử dụng cho rất nhiều sản phẩm như phân bón, thuốc nổ và nó còn được ứng dụng vào nhiều lĩnh vực công nghiệp khác.

Nghiên cứu cấu tạo của phân tử NH4NO3
Các nhà hóa học đã mất nhiều thời gian để nghiên cứu ra cấu tạo trong phân tử của Amoni Nitrat. Sau nhiều thí nghiệm, kết hợp với các công thức hóa học, người ta đã xác định được cấu tạo của NH4NO3 bao gồm: 1 nguyên tử Nitơ ở phần đỉnh, liên kết với 3 nguyên tử Hidro bằng cộng hóa trị, 3 nguyên tử này xếp thành hình tam giác ở đáy.
Hiện nay, trong các chương trình học của học sinh, người ta cũng cho vào một số hợp chất, vì vậy nếu ai học tốt môn hóa có thể viết được ngay phương trình hóa học của hợp chất này. Từ đó hiểu hơn về các liên kết và cấu tạo của nó.
Tìm hiểu tính chất hóa học, vật lý của Amoni Nitrat
Nghiên cứu về tính chất vật lý và tính chất hóa học của Amoni Nitrat (AN) sẽ giúp ích cho bạn trong việc nhận biết hợp chất này trong đời sống. Hiểu được các tính chất của nó để có thể sử dụng một cách đúng đắn nhất, tránh các trường hợp đáng tiếc xảy ra.
Tính chất vật lý của NH4NO3
Theo như nghiên cứu, Amoni Nitrat là hợp chất có tính rắn, có thể nhìn thấy bằng mắt thường, nó có màu trắng. Khi được đặt trong một nhiệt độ và áp suất tiêu chuẩn, AN có khả năng hút ẩm dưới dạng tinh thể. Vì vậy, một số nơi đã sử dụng hợp chất này cho vai trò hút ẩm.
Khi cho AN vào nước sẽ thấy nó tan ra với tốc độ nhanh, tan nhiều. Để đốt AN đến độ nóng chảy thì cần 169,6 độ C. Bên cạnh đó, nó sẽ sôi khi đạt tới nhiệt độ 210 độ C, nếu nâng nhiệt độ lên một chút là 230 độ C sẽ khiến Amoni Nitrat phân hủy và đặc biệt là tan chảy khi có nhiệt độ trên 325 độ C. Tỷ khối của AN là 1,73g/cm3.

Tính chất hóa học của NH4NO3
Tính chất hóa học là những phản ứng của hợp chất Amoni Nitrat với những chất khác, tìm ra được bản chất về mặt hóa học của nó. Trải qua nhiều thí nghiệm, rút ra được rằng AN hoàn toàn có thể nổ tung khi nhiệt độ nung nóng lên tới 260 độ C, tùy nhiên còn tùy thuộc vào tốc độ gia nhiệt của nó. Người ta phân tích được rằng đầu tiên, NH4NO3 có tính bazơ yếu, do trong cấu tạo phân tử không có sự liên kết của cặp e.
Amoni Nitrat có thế bị nhiệt phân khi bị tác động bởi nhiệt độ cao từ 190 – 245 độ C. Khi này, nó sẽ sinh ra bọt khí bởi trong quá trình phản ứng đã sinh ra Đinitơ Oxit (N2O). Phương trình phản ứng cụ thể là: NH4NO3 ⟶ 2H2O + N2O. Bên cạnh đó, hợp chất này còn có thể tạo ra các chất khác nếu cho tác dụng với axit HCl và H2SO4.
Phương trình hóa học của quá trình này là: HCl + NH4NO3 ⟶ HNO3 + NH4Cl. Khi cho tác dụng với axit H2SO4 thì phương trình viết ra là: H2SO4 + 2NH4NO3 ⟶ (NH4)2SO4 + 2HNO3. Hợp chất này còn có thể tác dụng với bazơ để tạo ra muối và hidroxide như: KOH + NH4NO3 ⟶ H2O + NH3 + HNO3 hay NH4NO3 + NaOH ⟶ NH4OH + NaNO3. Ngoài ra, Amoni Nitrat tác dụng được với muối để tạo ra các muối khác.
Một số phương trình hóa học của NH4NO3
Đầu tiên phải nhắc đến phương trình tác dụng giữa NH4NO3 và muối Na3PO4, Be(NO3)2 sẽ tạo ra 3NaNO3 và Be(NH4PO4). Quá trình người ta làm phân hủy Amoni Nitrat cũng có những phương trình khác nhau khi cho phân hủy ở nhiệt độ khác nhau.
- Phương trình diễn ra ở nhiệt độ 180 độ C: NH4NO3 = HNO3 + NH3.
- Phương trình diễn ra ở nhiệt độ 250 độ C: NH4NO3 = 2H2O + N2O.
- Phương trình diễn ra ở nhiệt độ trên 300 độ C: NH4NO3 = 2N2 + O2 + 4H2O.
- Phương trình nổ AN trong điều kiện không gian kín: 4NH4NO3 = 2NO2 + 3N2 + 8H2O.
Làm thế nào để điều chế NH4NO3?
Được biết, hợp chất Amoni Nitrat này có thể được điều chế từ những phản ứng trung hòa amoniac và axit nitric. Ngoài ra, sử dụng các chất gia dụng bình thường, phổ biến cũng có thể điều chế ra được hợp chất này. Dưới đây là những phản ứng thường được sử dụng để cho ra sản phẩm là NH4NO3.
- 2NO2 + H2O + 2NH3 ⟶ NH4NO3 + NH4NO2.
- NH4CIO4 + HNO3 ⟶ HClO4 + NH4NO3.
- AgNO3 + NH3 + C2H2 ⟶ C2Ag2 + NH4NO3.
- NH3 + AgNO3 + C4H6 ⟶ NH4NO3 + C4H5Ag.
- 2HNO3 + 8H ⟶ NH4NO3 + 3H2O.
- 2NH4OH + N2O5 ⟶ 2NH4NO3 + H2O.
Có thể ứng dụng Amoni Nitrat vào cái gì?
Đây là một hợp chất hóa học được sử dụng trong rất nhiều lĩnh vực. Nhìn vào những phương trình hóa học của nó cũng có thể thấy rằng chất hóa học này tác dụng được với rất nhiều loại chất khác. Dựa vào tính chất hóa học của nó, các nhà khoa học đã cho ra nhiều sản phẩm với sự góp mặt của Amoni Nitrat.
Ứng dụng vào ngành nông nghiệp
Những ai làm việc trong ngành nông nghiệp chắc chắn sẽ biết về hợp chất này. Bởi đây là một trong những nguyên liệu vô cùng quen thuộc để sản xuất ra phân bón. Trong loại phân bón này sẽ có hàm lượng Nitơ vừa đủ, giúp cây phát triển tốt. Loại phân bón được tạo nên từ Amoni Nitrat được sử dụng nhiều do tính chất dễ hấp thu của nó. Cây trồng khi dùng loại này đều khỏe mạnh, nhanh phát triển, nâng cao năng suất kinh tế.
Bên cạnh đó, loại phân bón Amoni còn có nhiều ưu điểm như là không làm chua đất, giúp nhiều cây trồng như khoai, ngô, mía, bông, đay được bổ sung thêm Nitrat. Để tăng thêm hiệu quả, người ta thường trộn phân bón Nitrat với nhiều loại phân bón khác để cây hấp thụ tốt.
Các ưu điểm như dễ xử lý, chứa nhiều chất dinh dưỡng khiến loại phân bón Amoni Nitrat này được nhiều người tin dùng. Trong điều kiện ẩm ướt, loại phân bón này còn có thể hòa tan và di chuyển ra xa gốc cây, không chỉ thế, nitrat còn giải phóng nitơ oxit khi độ ẩm tăng cao, không tồn tại lâu gây hại cho cây.

Sử dụng NH4NO3 làm thuốc nổ
Như đã nói, Amoni Nitrat có khả năng cháy nổ cực cao vì tính oxi hóa mạnh của nó. Vì vậy, người ta đã ứng dụng tính chất này vào công đoạn sản xuất thuốc nổ, tạo ra ANFO. Loại thuốc nổ này thường được các công ty khai thác mỏ, đá và nhiên liệu sử dụng để cho nổ các khối đá lớn, sử dụng trong việc đào mỏ, đào đường xuyên núi,…
Dân xây dựng rất hay tận dụng loại thuốc nổ này để tăng hiệu quả làm việc. Tại Mỹ, đã có những giai đoạn chất nổ này chiếm tới 80% tổng số chất nổ đang có và đang được sử dụng. Về sau, khi sản xuất thuốc nổ ngày càng đại trà, các vụ việc cháy nổ do Amoni Nitrat cũng tăng cao. Chính vì vậy, nhiều quốc gia đã loại bỏ hóa chất này, không cho sản xuất thuốc nổ NH4NO3 nữa.
Lý giải nguyên nhân NH4NO3 phát nổ?
Chất hóa học này khá dễ cháy nổ, tuy nhiên nếu đặt Amoni Nitrat một mình thì nó sẽ ít có khả năng phát nổ được. Dù vậy, các điều kiện để chất này chuyển thành chất nổ lại lại khá dễ dàng, dù có thể không có chất xúc tác hay những nhiên liệu phụ.
Cụ thể quá trình Amoni Nitrat phát nổ là khi chúng tự “ủ”, việc để chất này lâu trong thời tiết nóng ẩm sẽ giống như đem phân bón đi ủ. Bản chất của NH4NO3 cũng đã giàu năng lượng sẵn, khi chất này dần phân hủy, nó sẽ tạo ra một lượng nhiệt, khi gom đủ nhiệt thì NH4NO3 hoàn toàn có thể bốc cháy. Càng cháy, chất này sẽ sinh ra nhiều O2 – chất khí này lại giúp duy trì sự cháy được lâu hơn. Đó là lý do vì sao các đám cháy từ Amoni Nitrat có thể lan rất rộng.
Nhưng đó mới chỉ dừng ở mức cháy, để nổ được, các khí được hình thành từ vụ cháy phải bị niêm kín trong NH4NO3 nóng chảy. Việc oxy thoát ra từ một chất lỏng có nhiệt độ cao, lại không phải nước là rất khó, chính vào thời điểm này, khi chất khí trong chất lỏng của AN quá nhiều, nó buộc phải nổ tung để giải phóng toàn bộ khí.

Sử dụng và bảo quản AN cần lưu ý gì?
Để sử dụng được chất Amoni Nitrat và bảo quản nó một cách an toàn thì bạn cần phải chú ý vào những tính chất đã kể trên của nó. Việc giữ AN trong nhà sẽ nguy hiểm nếu bạn phạm phải một trong những lỗi sau:
- Bọc NH4NO3 quá kỹ.
- Để hợp chất Amoni Nitrat ở nơi có nhiệt độ cao, ẩm, lại bọc trong lớp nilon không thoáng khí.
- Để hợp chất gần hoặc tiếp xúc với các loại bột kim loại và chất hữu cơ.
Nếu bạn tránh được các trường hợp này, kết hợp cùng với việc bảo quản Amoni Nitrat ở nhiệt độ vừa phải, thoáng khí thì trường hợp nó phát nổ sẽ có phần trăm xảy ra nhỏ hơn rất nhiều.
Kết luận
Amoni Nitrat là một chất được ứng dụng rất nhiều trong khoa học, nông nghiệp, quân sự, xây dựng nhưng cũng là một chất nguy hiểm. Vì vậy, chỉ những cơ sở đạt chuẩn về môi trường mới được lưu trữ chất này.