Thông tin cơ bản về những tính chất hóa học của h2s như thế nào. Tạo các phản ứng ra sao với các chất hóa học để từ đó ứng dụng cho các ngành công nghiệp khác nhau.
Khí H2S là chất khí rất độc hại cho con người, động vật, thực vật và cả môi trường. Tuy là chất khí không có màu nhưng lại có mùi rất khó chịu (được mô tả như mùi trứng thối). Hằng năm chất khí này được đưa vào khí quyển với 1 lượng khá lớn từ cả nguồn gốc tự nhiên và nguồn nhân tạo.
Tính chất của h2s – hidro sunfua
Dưới đây là 1 số tính chất của h2s
- Khí H2S không màu nặng hơn không khí
- Là khí có mùi thối khó chịu với mùi trứng thối đặc trưng và rất độc.
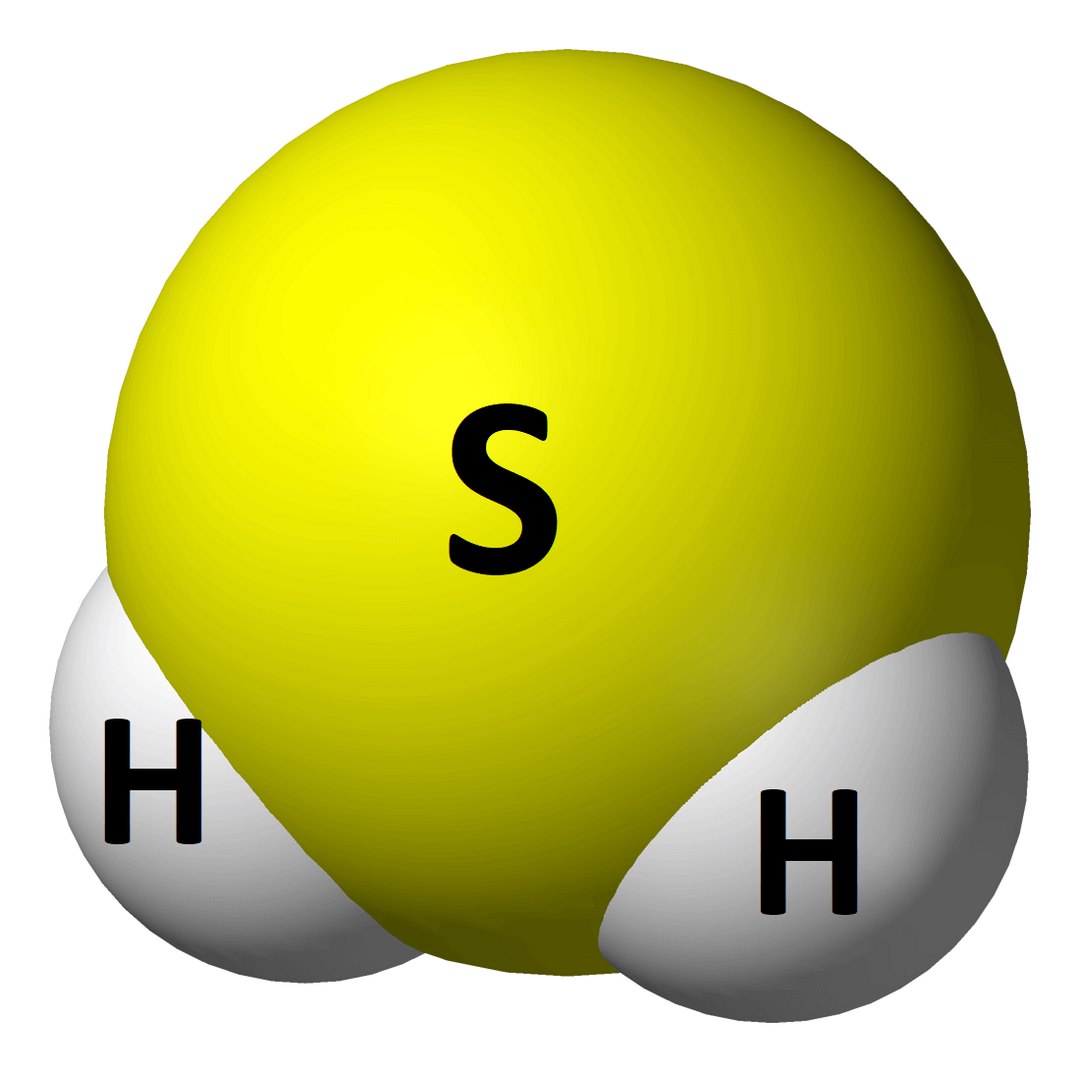
- Cấu trúc phân tử của chất H2S tương tự như cấu trúc phân tử của nước( H2) là đều bị phân cực .
- Tuy nhiên H2S có khả năng tạo thành liên kết Hiđro yếu hơn nước. H2S là chất khí ít tan trong nước nhưng lại tan nhiều trong dung môi hữu cơ.

Có thể bạn quan tâm:
- Giới thiệu phương pháp điều chế H2S trong phòng thí nghiệm
- Tổng hợp những ứng dụng của H2S có thể bạn không biết
- Khí H2S có gây hại gì? – cách nhận biết H2S độc ra sao?
Tính chất hóa học của H2S
H2s có tính axit: Tính chất hóa học của h2s
Tính chất hóa học của h2s đầu tiên mà chúng ta muốn nhắc đến là h2s có tính axit yếu.
♦ Khí Hiđro sunfua có thể tan trong nước như được nhắc ở trên và tạo thành dung dịch axit rất yếu có tên là axit sunfuhiđric, nó hoạt động yếu hơn cả axit cacbonic.
♦ Axit sunfuhiđric tác dụng với dung dịch kiềm sẽ tạo nên 2 loại muối: muối trung hòa và muối axit.
Axit H2S có tính khử mạnh
Hidro sunfua có tính chất hóa học đặc trưng là có tính khử mạnh là tính chất hóa học của h2s thứ 2 mà chúng ta cần nói đến.
Vì trong phân tử H2S lưu huỳnh có số oxi hóa thấp nhất (-2) nên nó là chất khử mạnh có thể tác dụng hầu hết các chất oxy hóa cho sản phẩm có số oxh cao hơn. Trong hợp chất H2S, có số oxi hóa của nguyên tố lưu huỳnh nằm ở mức thấp nhất là −2.
Tùy thuộc vào bản chất và nồng độ của chất oxi hóa tham gia các phản ứng hóa học, cũng như mức nhiệt độ mà nguyên tố lưu huỳnh có thể bị oxi hóa thành dạng lưu huỳnh tự do (S0). Hoặc chuyển thành lưu huỳnh với số oxi hóa +4 (S+4), dạng lưu huỳnh có số oxi hóa +6 (S+6).
Các phản ứng của h2s
Khí H2S tác dụng với O2 có thể tạo ra S hoặc SO2 tùy theo cách tiến hành phản ứng và lượng oxi:
♦ 2H2S + 3O2 → 2H2O + 2SO2 (nếu dư oxi)
♦ 2H2S + O2 →2H2O + 2S
Ở nhiệt độ cao, khí H2S sẽ bị cháy trong không khí với ngọn lửa có màu xanh nhạt, khí H2S bị oxi hóa thành SO2:
♦ 2H2S + 3O2 -> 2H2O + 2SO2
Khi tác dụng với clo thì H2S có thể tạo S hay H2SO4 tùy theo từng điều kiện phản ứng:
♦ H2S+4Cl2 + 4H2O → 8HCl + H2SO4
♦ H2S +Cl2 → 2 HCl + S (khí clo gặp khí H2S)
Dung dịch H2S có tính axit yếu ở 2 nấc : Khi tác dụng với dung dịch kiềm thì có thể tạo muối axit hoặc tạo muối trung hoà
♦ H2S + NaOH → NaHS + H2O
♦ H2S + NaOH → Na2S + H2O
Cách điều chế H2S phổ biến hiện nay
Điều chế H2S từ tự nhiên
♦ Khí này đa số sinh ra trong tự nhiên và khí thải của các ngành công nghiệp như đã nhắc ở trên. Hidro sunfua thường được điều chế từ sự phân hủy vi sinh vật của các chất hữu cơ khi không có O2 (hay còn gọi là quá trình phân hủy kỵ khí)
♦ H2S cũng tồn tại trong khí núi lửa, khí tự nhiên
♦ Trong phòng thí nghiệm thì người ta điều chế chất khí này bằng cách cho dung dịch axit clohiđric phản ứng với sắt (II) sunfua:
♦ FeS+2HCl→FeCl2+H2S↑
♦ Hoặc điều chế h2s từ s
♦ Một số sunfua kim loại và phi kim khi tác dụng với nước sẽ tạo ra hydro sunfua

Có thể bạn quan tâm:
- SO2 và một số ứng dụng có ích trong cuộc sống con người
- Clo – phi kim hoạt động hóa học mạnh có tính ứng dụng cao
Điều chế H2S trong công nghiệp
Sản xuất H2S khi tách khỏi khí chua – đây là khí tự nhiên có hàm lượng H2S cao. Ngoài ra, ta có thể sản xuất bằng cách xử lý hydro bằng lưu huỳnh nguyên tố nóng chảy ở khoảng 450 °C.
Trên đây là những tính chất hóa học của h2s mà chúng ta cần tìm hiểu. H2S là loại khí độc tồn tại xung quanh chúng ta. Chính vì vây hãy tìm hiểu cách phòng tránh nó nhé.